Los números cuánticos son unos números asociados a magnitudes físicas conservadas en ciertos sistemas cuánticos. En muchos sistemas el estado del sistema puede ser representado por un conjunto de números, los números cuánticos, que se corresponden con valores posibles deobservables que conmutan con el Hamiltoniano del sistema. Los números cuánticos permiten caracterizar los estados estacionarios, es decir losestados propios del sistema.
En física atómica, los números cuánticos son valores numéricos discretos que indican las características de los electrones en los átomos, esto está basado en la teoría atómica de Niels Bohr que es el modelo atómico más aceptado y utilizado en los últimos tiempos por su simplicidad.
En física de partículas, también se emplea el término números cuánticos para designar a los posibles valores de ciertos observables o magnitud física que poseen un espectro o rango posible de valores discretos
Conjunto de números cuánticos
El conjunto de números cuánticos más ampliamente estudiado es el de un electrón simple en un átomo: a causa de que no es útil solamente en química, siendo la noción básica detrás de la tabla periódica, valencia y otras propiedades, sino también porque es un problema resoluble y realista, y como tal, encuentra amplio uso en libros de texto.
En mecánica cuántica no-relativista, el hamiltoniano atómico de un átomo hidrogenoide consiste de la energía cinética del electrón y la energía potencial debida a la fuerza de Coulomb entre el núcleo y el electrón. En átomos más generales es necesario incluir la energía de interacción entre diferentes electrones. La energía cinética puede ser separada en una parte debida al momento angular, J, del electrón alrededor del núcleo, y el resto. Puesto que el potencial es esféricamente simétrico, el Hamiltoniano completo conmuta con J2. A su vez J2 conmuta con cualquiera de los componentes del vector momento angular, convencionalmente tomado como Jz. Estos son los únicos operadores que conmutan mutuamente en este problema; por lo tanto, hay tres números cuánticos. Adicionalmente hay que considerar otra propiedad de las partículas denominada espínque viene descrita por otros dos números cuánticos.
En particular, se refiere a los números que caracterizan los estados propios estacionarios de un electrón de un átomo hidrogenoide y que, por tanto, describen los orbitales atómicos. Estos números cuánticos son:
- I) El número cuántico principal n Este número cuántico está relacionado tanto con la energía como con la distancia media entre el núcleo y el electrón, medida en niveles energéticos, aunque la distancia media en unidades de longitud también crece monótonamente con n. Los valores de este número, que corresponde al número del nivel energético, varían teóricamente entre 1 e infinito, pero solo se conocen átomos que tengan hasta 8 niveles energéticos en su estado fundamental ya que el número atómico y el número cuántico principal se relacionan mediante 2n2 = Z < 110.
- II) El número cuántico secundario o azimutal (l = 0,1,2,3,4,5,...,n-1), indica la forma de los orbitales y el subnivel de energía en el que se encuentra el electrón. Un orbital de un átomo hidrogenoide tiene l nodos angulares y n-1-l nodos radiales. Si:
- l = 0: Subórbita "s" (forma circular) →s proviene de sharp (nítido) (*)
- l = 1: Subórbita "p" (forma semicircular achatada) →p proviene de principal (*)
- l = 2: Subórbita "d" (forma lobular, con anillo nodal) →d proviene de difuse (difuso) (*)
- l = 3: Subórbita "f" (lobulares con nodos radiales) →f proviene de fundamental (*)
- l = 4: Subórbita "g" (*)
- l = 5: Subórbita "h" (*)
- (*) Para obtener mayor información sobre los orbitales vea el artículo Orbital.
- III) El número cuántico magnético (m, ml), Indica la orientación espacial del subnivel de energía, "(m = -l,...,0,...,l)". Para cada valor de l hay 2l+1 valores de m.
- IV) El número cuántico de espín (s, ms), Describe el giro del electrón en torno a su propio eje, en un movimiento de rotación. Este giro puede hacerlo sólo en dos direcciones, opuestas entre sí. Por ello, los valores que puede tomar el número cuántico de spin son -1/2 y +1/2. Dicho de otra manera, Cada electrón, en un orbital, gira sobre si mismo. Este giro puede ser en el mismo sentido que el de su movimiento orbital o en sentido contrario. Este hecho se determina mediante un nuevo número cuántico, el número cuántico se spin s, que puede tomar dos valores, 1/2 y -1/2.
El estado cuántico de un electrón está determinado por sus números cuánticos:
| nombre | símbolo | significado orbital | rango de valores | valor ejemplo |
|---|---|---|---|---|
| número cuántico principal |  | shell o capa |  |  |
| número cuántico secundario o azimutal (momento angular) |  | subshell o subcapa | 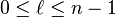 | para  : : |
| número cuántico magnético, (proyección del momento angular) |  | energía shift |  | para : :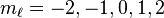 |
| número cuántico proyección de espín |  | espín |  | para un electrón, sea:  |
Con cada una de las capas del modelo atómico de Bohr correspondía a un valor diferente del número cuántico principal. Más tarde introdujeron los otros números cuánticos yWolfgang Pauli, otro de los principales contribuidores de la teoría cuántica, formuló el celebrado principio de exclusión basado en los números cuánticos, según el cual en un átomo no puede haber dos electrones cuyos números cuánticos sean todos iguales. Este principio justificaba la forma de llenarse las capas de átomos cada vez más pesados, y daba cuenta de por qué la materia ocupa lugar en el espacio.
Desde un punto de vista mecano-cuántico, los números cuánticos caracterizan las soluciones estacionarias de la Ecuación de Schrödinger.
No es posible saber la posición y la velocidad exactas de un electrón en un momento determinado, sin embargo, es posible describir dónde se encuentra. Esto se denominaprincipio de incertidumbre o de Heisenberg. La zona que puede ocupar un electrón dentro de un átomo se llama orbital atómico. Existen varios orbitales distintos en cada átomo, cada uno de los cuales tiene un tamaño, forma y nivel de energía específico. Puede contener hasta dos electrones que, a su vez, tienen números cuánticos de espínopuestos.
No hay comentarios:
Publicar un comentario